Höchstleistungsrechenzentrum Stuttgart
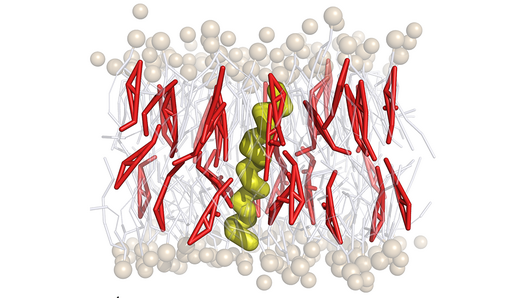
In einem kürzlich in der Fachzeitschrift Nature Communications veröffentlichten Artikel erläutern die Forschenden, wie die evolutionäre Molekulardynamik wichtige biophysikalische Prozesse an der Plasmamembran in Säugetierzellen erklären kann. Der Artikel stellt auch eine seit Langem vertretene Hypothese darüber in Frage, wie sich Cholesterin in der Nähe von Plasmamembranproteinen ansammelt. Darüber hinaus zeigt er einen ungewöhnlichen Mechanismus auf, der dieses Phänomen besser erklären könnte.
Cholesterin ist ein wichtiger Bestandteil der Plasmamembranen von Säugetieren und spielt in der Interaktion mit Proteinen eine wichtige Rolle bei Prozessen, die biochemische Signale in und aus den Zellen übertragen. Es gibt Hinweise darauf, dass eine abnormale Anreicherung von Cholesterin auch eine Rolle bei neurologischen Erkrankungen und Krebs spielen kann. Ein besseres Verständnis der Wechselwirkungen zwischen Cholesterin und Proteinen in der Plasmamembran könnte daher zu neuen Strategien für die Entwicklung von Medikamenten verhelfen.
Seit 2009 deuten Daten darauf hin, dass Membranproteine Cholesterin am Aminosäuremotiv CRAC (Cholesterol Recognition/Interaction Amino Acid Consensus) und dessen Umkehrung CARC anziehen. Diese Beobachtung legt nahe, dass eine genetische Sequenz und die daraus resultierende 3D-Proteinstruktur gut zu Cholesterinmolekülen passen, diese anziehen und an Ort und Stelle halten. So interessant diese Hypothese auch ist, wurden diese Motive jedoch nur vage definiert. Forschende konnten bislang nicht schlüssig nachweisen, dass Cholesterin an solchen Stellen an Proteine binden kann.
„Das Konzept, dass Cholesterinmoleküle an CRAC- und CARC-Motive binden, basiert auf der Vorstellung, dass es eine spezifische Anziehungskraft zwischen Liganden und Proteinen gibt“, erklärte Prof. Risselada. „Mithilfe von Röntgenkristallographie kann man beobachten, wie Cholesterin an andere Stoffe bindet. Eine Aufklärung der Struktur der CRAC-/CARC-Bindung war jedoch bisher nicht möglich. Als wir mit unserer Forschung begannen, wollten wir beweisen, dass Evo-MD durch die Wiederherstellung eines bekannten Motivs funktioniert. Überraschenderweise zeigte sich, dass das Motiv nicht für die Anziehung von Cholesterin verantwortlich war. Stattdessen führte es zu einer besseren Hypothese, warum dies geschieht.“
Risselada und der Postdoktorand Dr. Jeroen Methorst wollten die Natur der Cholesterinansammlung mittels Evo-MD besser verstehen. Konkret untersuchten sie thermodynamische Kräfte, die bestimmen, wie stark ein Cholesterinmolekül von einem Signalprotein angezogen wird, das die Plasmamembran durchspannt.
In einem Computeralgorithmus generierte Evo-MD zunächst eine große Menge zufälliger Aminosäuresequenzen – die genetischen Bausteine von Proteinen. Anschließend bewertete Evo-MD jede Sequenz daraufhin, inwieweit sie Cholesterin anziehen kann, und wies ihr einen Fitness-Score zu. Diejenigen, die am ehesten mit Cholesterin interagierten, erhielten einen höheren Score. Die Sequenzen, bei denen dies weniger wahrscheinlich war, wurden mit einem niedrigeren Score bewertet.
Nach Abschluss einer Runde wiederholte sich der gesamte Prozess, wobei in der zweiten Runde die besten Sequenzen aus der vorherigen Runde als Ausgangspunkt für die nächste Runde dienten. Der Algorithmus wählte erneut Sequenzen mit hoher Fitness aus und kombinierte sie anders, um eine neue Population aufzubauen. Dieser als „genetischer Algorithmus“ bezeichnete Prozess ahmt die Weitergabe von genetischem Material von Eltern an Kinder nach, führt jedoch gleichzeitig zufällige Veränderungen in den Aminosäuresequenzen ein, die eine bloße Kopie der genetischen Informationen zwischen den Generationen verhindern.
Um den Fitness-Score für jede Aminosäuresequenz zu generieren, verwendeten die Forschenden Molekulardynamik (MD). Diese rechenintensive Methode nutzt physikalische Prinzipien, um Wechselwirkungen zwischen Molekülen bis auf die atomare Ebene hin zu simulieren. Unter Anwendung von MD-Simulationen untersuchte das Team um Risselada, inwieweit Cholesterin und Transmembranmotive interagieren können. Konkret betrachteten sie Kraftfelder und quantifizierten dabei die Energie innerhalb des Systems, die sich aus der Anordnung von Molekülen und Atomen im Raum ergibt.
Ähnlich wie bei einer Spezies, die sich erfolgreich an ihre Umgebung anpasst, führt die wiederholte Durchführung dieses Zyklus die Evolution zum Ziel einer optimalen Fitnesslösung. Dank der Kombination aus Zufallsstichproben und einem datengesteuerten Ansatz des Reinforcement Learning maximiert Evo-MD die Anziehung zwischen Proteinen und Cholesterin deutlich schneller und effizienter, als wenn jede mögliche Kombination von Aminosäuresequenzen einzeln getestet würde. (Im untersuchten Beispiel wären dafür 2010 Varianten zu prüfen gewesen!) Zugleich bindet der Algorithmus Molekulardynamik-Simulationen ein. So beruhen die Vorhersagen zu den Wechselwirkungen zwischen Cholesterin und Proteinen auf etablierten biophysikalischen Prinzipien und bleiben wissenschaftlich fundiert.
Die Forschenden fanden heraus, dass Evo-MD nach der Simulation von etwa 128 einzelnen Aminosäuresequenzen über 40 Iterationen zu einem optimalen Fitnesswert konvergiert, bei dem die besten Sequenzen eine stabile Wechselwirkung zwischen Protein- und Cholesterinmolekülen ermöglichen. „Das Interessante an einem datengesteuerten Ansatz ist, dass er eine Lösung findet, die am besten zu den verfügbaren Daten passt“, erklärte Risselada. „Doch dann stellt sich die Frage: Warum ist das die Lösung?“
Überraschenderweise stellten die Forscher bei der Untersuchung der optimalen Protein-Cholesterin-Wechselwirkungen fest, dass CRAC-/CARC-Motive allein kein Cholesterin anziehen können, da sie Aminosäuresequenzen enthalten, die es aktiv abstoßen. Stattdessen deuten die Ergebnisse darauf hin, dass in den CRAC-/CARC-umgebenden Proteinstrukturen ein feines Gleichgewicht zwischen denen besteht, die Cholesterin anziehen, und denen, die es abstoßen. Dadurch entsteht ein komplexeres Zusammenspiel thermodynamischer Kräfte, das das Lipid an Ort und Stelle hält. Aus dieser Perspektive bindet sich Cholesterin also nicht an CRAC-/CARC-Motive, sondern benachbarte Strukturen im Protein erleichtern die Cholesterinakkumulation. Experimente mit Kernspinresonanz-Scans und zellulären Nachweisverfahren bestätigten, dass diese Erklärung wahrscheinlicher ist, und lieferten weitere Details zu den genau beteiligten Aminosäureresten.
„Normalerweise verbinden sich Moleküle, weil ihre Formen zusammenpassen. In diesem Fall ist jedoch klar, dass der Mechanismus nicht normal ist“, sagte Risselada. „Diese Reaktion hier lässt sich als membranvermittelter Effekt einstufen, der einige Zusammensetzungsmerkmale festlegt, aber auch viel Flexibilität ermöglicht. Das Protein induziert einen hochenergetischen Zustand in der Membran, der eine effektive Cholesterinanziehung bewirkt.“
Evo-MD muss viele verschiedene Aminosäuresequenzen gleichzeitig berechnen. Nur so lässt sich die gesamte Bandbreite möglicher Lösungen erfassen. Daher müssen viele Simulationen parallel ausgeführt werden, wobei bis zu Tausende von Rechenkernen zum Einsatz kommen. Aus diesem Grund war eine effiziente Durchführung des Forschungsprojekts nur mit dem Supercomputer Hawk des HLRS und anderen Großrechnern möglich. Die Forschenden erhielten auf mehreren Computern konsistente Ergebnisse, was ihr Vertrauen in die Zuverlässigkeit ihrer Methode stärkte.
Im Laufe dieses Projekts verbesserte das Team den Evo-MD-Algorithmus, um die Rechenkapazitäten effizienter zu nutzen. Zunächst mussten alle Simulationen einer Generation von Aminosäuresequenzen abgeschlossen sein, bevor die nächste Generation beginnen konnte. In dieser Zeit standen jedoch viele Rechenkerne im Leerlauf, weil sie auf den Abschluss anderer Berechnungen warteten. Heute verwendet das System einen komplexeren Arbeitsablauf, bei dem sich die Generationen nicht streng chronologisch entwickeln, sondern zwischen Pools potenzieller Aminosäuresequenzen hin- und herspringen. Diese Vorgehensweise verbessert die Lastverteilung und die parallelen Rechenkapazitäten des HPC lassen sich besser nutzen.
Aktuell wendet das Team von Risselada Evo-MD auf weitere Fragestellungen an, unter anderem die Verwendung evolutionärer Schemata zur Untersuchung der Wechselwirkungen zwischen kleinen Molekülen, die viel komplexere Systeme bilden.
„Viele Forschungsgruppen, die maschinelles Lernen einsetzen, sind sehr pragmatisch und konzentrieren sich auf strukturbasierte Optimierung für pharmazeutische Anwendungen“, erklärte Rissealada. „Evo-MD ermöglicht es uns, sehr dynamische Eigenschaften zu messen und einzigartige Grundlagenforschung zu betreiben.“
— Christopher Williams
Methorst J, Verwei N, Hoffmann, et al. 2025. Physics-based evolution of transmembrane helices reveals mechanisms of cholesterol attraction. Nat Commun. 16: 9275.
Hawk wurde vom Ministerium für Wissenschaft, Forschung und Kunst Baden-Württemberg und dem Bundesministerium für Forschung, Technologie und Raumfahrt über das Gauss Centre for Supercomputing (GCS) gefördert.